Entregas 24/48 H (días hábiles)
Envios GRATIS desde 29.95 € (compra)
Debido al apagón, los pedidos realizados del día 25 al 28 de abril saldrán todos a partir del día 29 de abril
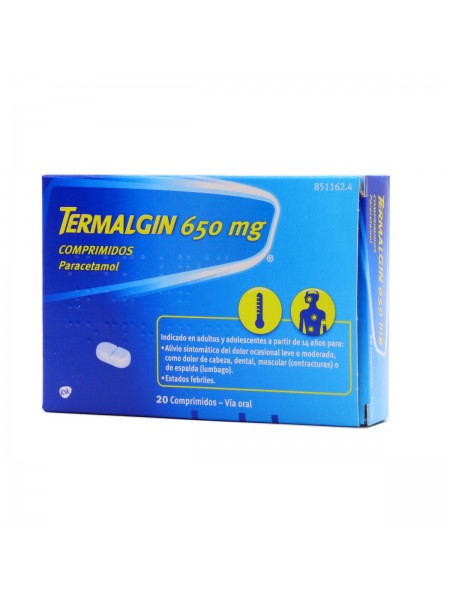
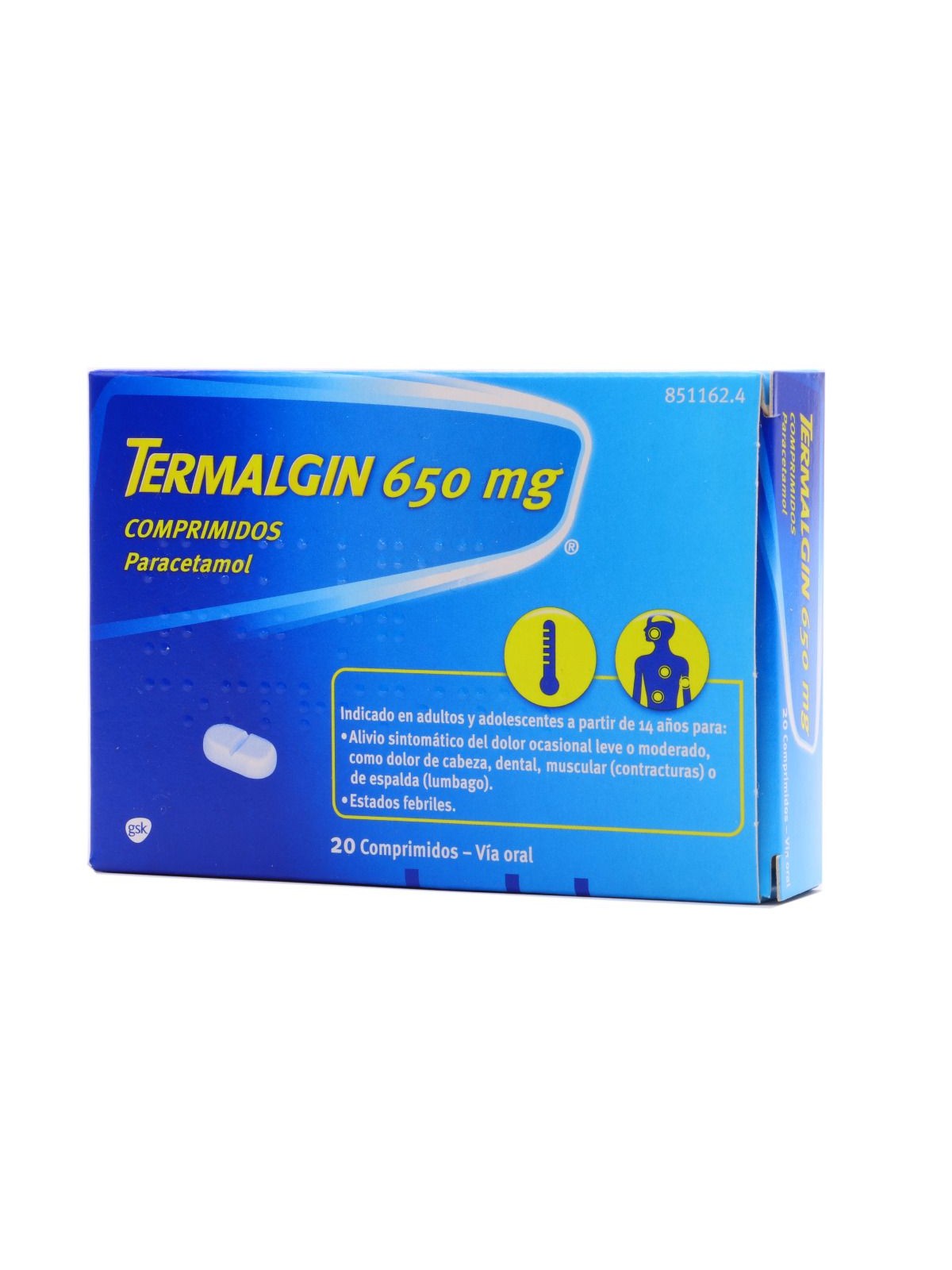
TERMALGIN 650 MG 20 COMPRIMIDOS
Termalgin 650mg está indicado en adultos y adolescentes a partir de 14 años para el alivio sintomático del dolor ocasional leve o moderado y estados febriles.
¿Tienes dudas? te ayudamos en el 976 73 46 08
ENVÍOS 4.95€ --- GRATIS a partir de 29.95 € (compra)
Entregas 24/48 H (días hábiles)
Pago 100% seguro - Métodos de pago: 
Termalgin 650mg está indicado en adultos y adolescentes a partir de 14 años para el alivio sintomático del dolor ocasional leve o moderado y estados febriles.
1. NOMBRE DEL MEDICAMENTO
Termalgin 650 mg comprimidos
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido contiene:
Paracetamol……. 650 mg
Para consultar la lista completa de excipientes, ver sección 6.1
3. FORMA FARMACÉUTICA
Comprimidos
Comprimidos blancos, oblongos y ranurados.
4. DATOS CLÍNICOS
4.1. Indicaciones terapéuticas
Este medicamento está indicado en adultos y adolescentes a partir de 14 años para el alivio sintomático del dolor ocasional leve o moderado y estados febriles.
4.2. Posología y forma de administración
Posología
• Adultos y adolescentes de 14 a 18 años:
Tomar 1 comprimido cada 4 – 6 horas, según necesidad, hasta un máximo de 4 comprimidos al día. No se excederá de 3g de paracetamol en 24 horas.
No exceder la dosis establecida. Utilizar la dosis mínima que resulte eficaz durante el menor periodo de tiempo posible.
Se debe evitar la administración de dosis altas de paracetamol durante periodos prolongados de tiempo ya que se incrementa el riesgo de daño hepático
Si el dolor se mantiene durante más de 5 días, la fiebre durante más de 3 días o bien el dolor o la fiebre empeoran o aparecen otros síntomas, se deberá evaluar la situación clínica.
Para el dolor de garganta no se debe administrar más de 2 días seguidos, sin evaluar la situación clínica.
• Pacientes con insuficiencia renal:
Debido a la dosis de paracetamol, no está indicado en este grupo de pacientes.
• Pacientes con insuficiencia hepática:
En caso de insuficiencia hepática no se excederá de 2 g/24 horas (3 comprimidos) y el intervalo mínimo entre dosis será de 8 horas (ver sección 4.4 advertencias y precauciones especiales de empleo).
•Población pediátrica:
Este medicamento está indicado en adultos y adolescentes a partir de 14 años. Los niños y adolescentes menores de 14 años no pueden tomar este medicamento.
Forma de administración
Este medicamento se administra por vía oral.
Los comprimidos deben tomarse con la ayuda de algún líquido, preferentemente agua.
Con la toma concomitante de paracetamol y alimentos el tiempo de absorción de paracetamol aumenta, debido a que los alimentos disminuyen la motilidad y el tiempo de transito gastrointestinal. Para un alivio rápido del dolor, tomar el medicamento sin comida, especialmente si ésta presenta un alto contenido en carbohidratos
4.3. Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
4.4. Advertencias y precauciones especiales de empleo
• Se debe evaluar la relación beneficio/riesgo, evitando tratamientos prolongados, en pacientes con anemia, afecciones cardíacas o pulmonares o con disfunción renal grave y hepática (en éste último caso, el uso ocasional es aceptable, pero la administración prolongada de dosis elevadas puede aumentar el riesgo de aparición de efectos adversos).
• La utilización de paracetamol en pacientes que consumen habitualmente alcohol (3 o más bebidas alcohólicas – cerveza, vino, licor... – al día) puede provocar daño hepático.
• En alcohólicos crónicos no se debe administrar más de 2 g/día de paracetamol repartidos en varias tomas.
• Se recomienda controlar a los pacientes asmáticos sensibles al ácido acetilsalicílico, debido a que se han descrito ligeras reacciones broncoespásticas cuando se les administra paracetamol (reacción cruzada). Aunque dichas reacciones solo se manifestaron en una minoría de dichos pacientes, en algunos casos se pueden producir reacciones graves, especialmente cuando se administran dosis altas de paracetamol. Su uso puede aumentar el riesgo de desarrollar asma en niños y adultos.
• Se debe limitar la automedicación con paracetamol cuando se está en tratamiento con anticonvulsivantes debido a que con el uso concomitante de ambos se potencia la hepatotoxicidad y se disminuye la biodisponibilidad del paracetamol, especialmente en tratamientos con dosis altas de paracetamol.
• Debe advertirse al paciente que evite el uso simultáneo de este medicamento con otros que contengan paracetamol, como por ejemplo medicamentos antigripales. En caso de administrarse otro medicamento que contenga paracetamol no se deberá exceder la dosis máxima de paracetamol de 3 g al día teniendo en cuenta el contenido del mismo de todos los medicamentos que utiliza el paciente.
• Los cuadros tóxicos asociados a paracetamol se pueden producir tanto por la ingesta de una sobredosis única o por varias tomas con dosis excesivas de paracetamol.
• Se han producido comunicaciones de casos de hepatotoxicidad con dosis diarias inferiores a 4 g.
• La sobredosis de paracetamol puede causar fallo hepático que puede derivar en trasplante hepático o muerte.
• En pacientes deshidratados y en estados con déficit de glutatión, por ejemplo, enfermedades hepáticas (incluido el síndrome de Gilbert) o estados de desnutrición puede aumentar el riesgo de daño hepatico con el uso de paracetamol. Asimismo se ha informado de casos de fallo hepático o disfunción hepática en pacientes con déficit de glutatión, como por ejemplo, en estados de malnutrición, anorexia y en pacientes con un bajo Índice de Masa Corporal.
4.5. Interacción con otros medicamentos y otras formas de interacción
El paracetamol se metaboliza intensamente en el hígado, por lo que puede interaccionar con otros medicamentos que utilicen sus mismas vías metabólicas o sean capaces de actuar, inhibiendo o induciendo, tales vías. Algunos de sus metabolitos son hepatotóxicos, por lo que la administración conjunta con potentes inductores enzimáticos (rifampicina, determinados anticonvulsivantes, etc.) puede conducir a reacciones de hepatotoxicidad, especialmente cuando se emplean dosis elevadas de paracetamol.
Entre las interacciones potencialmente más relevantes pueden citarse las siguientes:
• Alcohol etílico: potenciación de la toxicidad del paracetamol, por posible inducción de la producción hepática de productos hepatotóxicos derivados del paracetamol
• Anticoagulantes orales (acenocumarol, warfarina): La administración crónica de dosis de paracetamol superiores a 2 g/día con este tipo de productos, puede provocar una potenciación del efecto anticoagulante, por inhibición de la síntesis hepática de factores de coagulación. No obstante, dada la aparentemente escasa relevancia clínica de esta interacción en la mayoría de los pacientes, se considera la alternativa terapéutica analgésica con salicilatos, cuando existe terapia con anticoagulantes. No obstante, la dosis y duración del tratamiento deben ser lo más bajo posibles, con monitorización periódica del INR.
• Anticonvulsivantes (fenitoína, fenobarbital, metilfenobarbital, primidona): disminución de la biodisponibilidad del paracetamol así como potenciación de la hepatotoxicidad a sobredosis, debido a la inducción del metabolismo hepático.
• Diuréticos del asa: los efectos de los diuréticos pueden verse reducidos, ya que el paracetamol puede disminuir la excreción renal de prostaglandinas y la actividad de la renina plasmática.
• Isoniazida: disminución del aclaramiento de paracetamol, con posible potenciación de su acción y/o toxicidad, por inhibición de su metabolismo hepático.
• Lamotrigina: disminución de la biodisponibilidad de lamotrigina, con posible reducción de su efecto, por posible inducción de su metabolismo hepático.
• Metoclopramida y domperidona: aumentan la absorción del paracetamol en el intestino delgado, por el efecto de estos medicamentos sobre el vaciado gástrico.
• Probenecid: incrementa la semivida plasmática del paracetamol, al disminuir la degradación y excreción urinaria de sus metabolitos.
• Propranolol: aumento de los niveles plasmáticos de paracetamol, por posible inhibición de su metabolismo hepático.
• Resinas de intercambio iónico (colestiramina): disminución en la absorción del paracetamol, con posible inhibición de su efecto, por fijación del paracetamol en intestino.
• Interferencias con pruebas analíticas:.
El paracetamol puede alterar los valores de las determinaciones analíticas de ácido úrico y glucosa.
4.6. Fertilidad, embarazo y lactancia
Embarazo:
Una gran cantidad de datos en mujeres embarazadas indican la ausencia de toxicidad fetal/neonatal o malformaciones congénitas. Los estudios epidemiológicos sobre el desarrollo neurológico de niños expuestos a paracetamol en el útero muestran resultados no concluyentes. Si es clínicamente necesario, puede utilizarse paracetamol durante el embarazo, pero debe usarse la dosis mínima eficaz durante el menor tiempo posible y con la menor frecuencia posible
Lactancia:
Aunque en la leche materna se han medido concentraciones máximas de 10 a 15 μg/ml (de 66,2 a 99,3 μmoles/l) al cabo de 1 o 2 horas de la ingestión, por parte de la madre, de una dosis única de 650 mg, en la orina de los lactantes no se ha detectado paracetamol ni sus metabolitos. La vida media en la leche materna es de 1,35 a 3,5 horas. No se han producido comunicaciones de efectos adversos en niños. Paracetamol se puede utilizar en mujeres en periodo de lactancia si no se excede la dosis recomendada. Se debe tener precaución en el caso de uso prolongado.
4.7. Efectos sobre la capacidad para conducir y utilizar máquinas
La influencia de Termalgin sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
No se ha descrito ningún efecto en este sentido.
4.8. Reacciones adversas
a. Informe del perfil de seguridad
Las reacciones adversas que más se han informado durante el periodo de utilización de paracetamol son: hepatotoxicidad, toxicidad renal, alteraciones en la fórmula sanguínea, hipoglucemia y dermatitis alérgica, por lo general, raras o muy raras.
Frecuencia
Raras (≥1/10.000,<1/1.000)
Trastornos vasculares: Hipotensión
Trastornos hepatobiliares: Niveles aumentados de transaminasas hepáticas
Trastornos generales y alteraciones en el lugar de administración: Malestar
Muy raras (<1/10.000)
Trastornos de la sangre y del sistema linfático Trombocitopenia, agranulocitosis, leucopenia, neutropenia, anemia hemolítica.
Trastornos del metabolismo y de la nutrición: Hipoglucemia
Trastornos hepatobiliares: Hepatotoxicidad (ictericia)
Trastornos renales y urinarios: Piuria estéril (orina turbia), efectos renales adversos (véase epígrafe 4.4. Advertencias y precauciones especiales de empleo)
Trastornos generales y alteraciones en el lugar de administración: Reacciones de hipersensibilidad que oscilan, entre otros, entre una simple erupción cutánea o una urticaria, angioedema, síndrome de Stevens Johnson, necrólisis epidérmica tóxica y shock anafiláctico
Desconocida ( no se pueden establecer a partir de los datos disponibles) Trastornos del sistema nervioso: Cefaleas inducidas por el abuso de analgésicos
En caso de observar la aparición de reacciones adversas, se deben notificar a los sistemas de Farmacovigilancia y, si fuera necesario, suspender el tratamiento.
Notificación de sospechas de reacciones adversas:
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es.
4.9. Sobredosis
La sintomatología por sobredosis incluye mareos, vómitos, pérdida de apetito, ictericia, dolor abdominal e insuficiencia renal y hepática. Si se ha ingerido una sobredosis debe tratarse rápidamente al paciente en un centro médico aunque no haya síntomas o signos significativos ya que, aunque éstos pueden causar la muerte, a menudo no se manifiestan inmediatamente después de la ingestión, sino a partir del tercer día. Puede producirse la muerte por necrosis hepática. Así mismo, puede aparecer fallo renal agudo.
La sobredosis de paracetamol puede causar fallo hepático que puede derivar en necesidad de trasplante hepático o muerte. Se ha observado pancreatitis aguda, usualmente con disfunción y toxicidad hepáticas.
La sobredosis de paracetamol se evalúa en cuatro fases, que comienzan en el momento de la ingestión de la sobredosis:
• FASE I (12 - 24 horas): náuseas, vómitos, diaforesis y anorexia.
• FASE II (24 - 48 horas): mejoría clínica; comienzan a elevarse los niveles de AST, ALT, bilirrubina y protrombina.
• FASE III (72 - 96 horas): pico de hepatotoxicidad; puede aparecer valores de 20.000 para la AST.
• FASE IV (7 - 8 días): recuperación.
Puede aparecer hepatotoxicidad. La mínima dosis tóxica es de más de 6 g en adultos y más de 100 mg/kg de peso en niños, en una sola toma. Dosis superiores a 20-25 g son potencialmente fatales. Los síntomas de la hepatotoxicidad incluyen náuseas, vómitos, anorexia, malestar, diaforesis, dolor abdominal y diarrea. La hepatotoxicidad no se manifiesta hasta pasadas 48 – 72 horas después de la ingestión. Si la dosis ingerida fue superior a 150 mg/kg o no puede determinarse la cantidad ingerida, hay que obtener una muestra de paracetamol sérico a las 4 horas de la ingestión. En el caso de que se produzca hepatotoxicidad, realizar un estudio de la función hepática y repetir el estudio con intervalos de 24 horas. El fallo hepático puede desencadenar encefalopatía, coma y muerte.
Vía intravenosa:
Se recomiendan 300 mg/kg de N-acetilcisteína (equivalentes a 1,5 ml/kg de solución acuosa al 20%; pH: 6,5), administrados por vía intravenosa durante un periodo de 20 horas y 15 minutos, según el siguiente esquema:
1. Adultos
• Dosis de ataque: 150 mg/kg (equivalentes a 0,75 ml/kg de solución acuosa al 20% de N- acetilcisteína; pH 6,5) lentamente por vía intravenosa o diluidos en 200 ml de dextrosa al 5%, durante 15 minutos.
• Dosis de mantenimiento:
a) Inicialmente se administrarán 50 mg/kg (equivalentes a 0,25 ml/kg de solución acuosa al 20% de N-acetilcisteína; pH: 6,5), en 500 ml de dextrosa al 5% en infusión lenta durante 4 horas.
b) Posteriormente, se administrarán 100 mg/kg (equivalentes a 0,50 ml/kg de solución acuosa al 20% de N-acetilcisteína; pH: 6,5), en 1000 ml de dextrosa al 5% en infusión lenta durante 16 horas.
Vía oral:
Es preciso administrar el antídoto de N-acetilcisteína antes de que transcurran 10 horas desde la sobredosificación.
Adultos
La dosis de antídoto recomendada para los adultos es:
• Una dosis inicial de 140 mg/kg de peso corporal
• 17 dosis de 70 mg/kg de peso corporal, una cada 4 horas
Cada dosis se debe diluir al 5% con una bebida de cola, zumo de uva, de naranja o agua, antes de ser administrada, debido a su olor desagradable y a sus propiedades irritantes o esclerosantes. Si la dosis se vomita en el plazo de una hora después de la administración, se debe repetir.
Si resulta necesario, el antídoto (diluido en agua) se puede administrar mediante la intubación duodenal.
5. PROPIEDADES FARMACOLÓGICAS
5.1. Propiedades farmacodinámicas
Grupo farmacoterapéutico: otros analgésicos y antipiréticos. Anilidas: Paracetamol.
Código ATC: N02BE01.
El paracetamol es un analgésico que también posee propiedades antipiréticas.
Se desconoce el mecanismo exacto de la acción del paracetamol, aunque se sabe que actúa a nivel del Sistema Nervioso Central y, en menor grado, bloqueando la generación del impulso doloroso a nivel periférico.
Se cree que el paracetamol aumenta el umbral del dolor inhibiendo la síntesis de prostaglandinas, mediante el bloqueo de ciclooxigenasas en el Sistema Nervioso Central (específicamente la COX-3). Sin embargo, el paracetamol no inhibe de forma significativa las ciclooxigenasas en los tejidos periféricos.
El paracetamol estimula la actividad de las vías serotoninérgicas descendentes que bloquean la transmisión de las señales nociceptivas a la médula espinal procedentes de tejidos periféricos.. En este sentido, algunos datos experimentales indican que la administración de antagonistas de diferentes subtipos de receptores serotoninérgicos administrados intraespinalmente son capaces de anular el efecto antinociceptivo del paracetamol.
La acción antitérmica está relacionada con la inhibición de la síntesis de PGE1 en el hipotálamo, órgano coordinador fisiológico del proceso de termorregulación.
5.2. Propiedades farmacocinéticas
Por vía oral la biodisponibilidad de paracetamol es del 75 – 85%. Se absorbe amplia y rápidamente, las concentraciones plasmáticas máximas se alcanzan en función de la forma farmacéutica con un tiempo de 0,5 a 2 horas.
La absorción del paracetamol tras la administración de TERMALGIN 1 g, polvo efervescente es rápida y completa. La concentración plasmática máxima se alcanza en promedio antes de los 30 minutos.
El grado de unión a proteínas plasmáticas es de un 10%. El tiempo que transcurre hasta lograr el efecto máximo es de 1 a 3 horas, y la duración de la acción es de 3 a 4 horas. El metabolismo del paracetamol experimenta un efecto de primer paso hepático, siguiendo una cinética lineal. Sin embargo, esta linealidad desaparece cuando se administran dosis superiores a 2 g. El paracetamol se metaboliza fundamentalmente en el hígado (90-95%), siendo eliminado mayoritariamente en la orina como un conjugado con el ácido glucurónico, y en menor proporción con el ácido sulfúrico y la cisteína; menos del 5% se excreta en forma inalterada. La semivida de eliminación es de 1,5-3 horas (aumenta en caso de sobredosis y en pacientes con insuficiencia hepática, ancianos y niños). Dosis elevadas pueden saturar los mecanismos habituales de metabolización hepática, lo que hace que se utilicen vías metabólicas alternativas que dan lugar a metabolitos hepatotóxicos y posiblemente nefrotóxicos, por agotamiento de glutatión.
5.3. Datos preclínicos sobre seguridad
El paracetamol, a dosis terapéuticas, no presenta efectos tóxicos y únicamente a dosis muy elevadas causa necrosis centrolobulillar hepática en los animales y en el hombre. Igualmente a niveles de dosis muy altos, el paracetamol causa metahemoglobinemia y hemolisis oxidativa en perros y gatos y muy rara vez en humanos.
Se han observado en estudios de toxicidad crónica, subcrónica y aguda, llevados a cabo con ratas y ratones, lesiones gastrointestinales, cambios en el recuento sanguíneo, degeneración del hígado y parénquima renal, incluso necrosis. Por un lado, las causas de estos cambios se han atribuido al mecanismo de acción y por otro lado, al metabolismo de paracetamol. Se ha visto también en humanos, que los metabolitos parecen producir los efectos tóxicos y los correspondientes cambios en los órganos. Además, se ha descrito casos muy raros de hepatitis agresiva crónica reversible durante el uso prolongado (ej. 1 año) con dosis terapéuticas. En el caso de dosis subtóxicas, pueden aparecer signos de intoxicación a las 3 semanas de tratamiento. Por lo tanto, paracetamol no deberá tomarse durante largos periodos de tiempo y tampoco a dosis altas.
Investigaciones adicionales no mostraron evidencia de un riesgo genotóxico de paracetamol relevante a las dosis terapéuticas, es decir a dosis no tóxicas.
Estudios a largo plazo en ratas y ratones no produjeron evidencia de tumores con dosis de paracetamol no hepatotóxicas.
Fertilidad: No se dispone de estudios convencionales que utilicen las normas actualmente aceptadas para la evaluación de la toxicidad para la reproducción y el desarrollo. Los estudios de toxicidad crónica en animales demuestran que dosis elevadas de paracetamol producen atrofia testicular e inhibición de la espermatogénesis; se desconoce la importancia de este hecho para su uso en humanos.
6. DATOS FARMACÉUTICOS
6.1. Lista de excipientes
Celulosa microcristalina
Almidón de maíz
Almidón de maíz pregelatinizado
Polivinilpirrolidona
Talco
Ácido esteárico
Ácido silícico coloidal.
6.2. Incompatibilidades
No procede.
6.3. Periodo de validez
5 años
6.4. Precauciones especiales de conservación
No se requieren condiciones especiales de conservación.
6.5. Naturaleza y contenido del envase
Envases de 20 comprimidos, acondicionados en tira de aluminio/PVC.
6.6. Precauciones especiales de eliminación y otras manipulaciones
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local (o se procederá a su devolución a la farmacia).
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
GLAXOSMITHKLINE CONSUMER HEALTHCARE S.A.
Parque Tecnológico de Madrid, Calle de Severo Ochoa, 2
28760 Tres Cantos, Madrid - España
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
43.990
9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN
Termalgin 650 mg comprimidos: 20.02.67 / 31.10.07
10. FECHA DE LA REVISIÓN DEL TEXTO
Diciembre 2020
Resolvemos tus dudas
Sobre este producto o cualquier otro, no dudes en ponerte en contacto con nuestros farmacéuticos y farmacéuticas de Farmacia Senante Actur, Zaragoza.
¡Consúltanos!